Différence entre l'acétone et l'acétate
- 974
- 184
- Juliette Lacroix
L'acétone est un type de cétone qui a la formule C3H6O ou CH3COCH3. L'acétate est un type d'anion qui a la formule CH3COO-.
Qu'est-ce que l'acétone?
Définition:
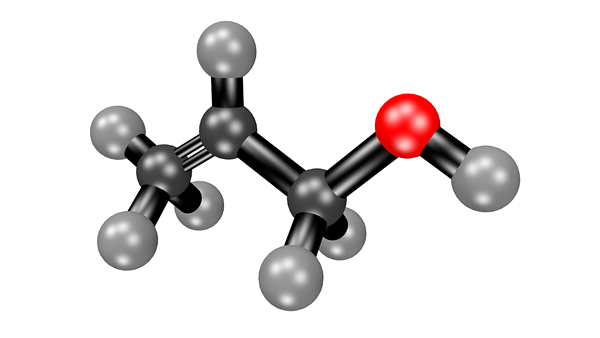
L'acétone est un type de molécule de cétone, et c'est un produit chimique qui a la formule moléculaire CH3COCH3.

Propriétés en acétone:
Ce produit chimique est une molécule appelée cétone et elle se trouve comme un liquide qui n'a pas de couleur. Le poids moléculaire de l'acétone est de 58.08 grammes par mol, et la substance a une odeur fruitée qui est très distinctive et l'acétone est également connue pour être inflammable.
Formation d'acétone:
L'acétone peut être formée artificiellement grâce à un processus spécial qui est appelé le processus hydroperoxyde de Cumene. Nous pouvons également faire de l'acétone dans notre corps lorsque les graisses sont décomposées et converties en corps cétone. Les personnes atteintes de diabète mal contrôlé peuvent éprouver une acidocétose qui peut être très dangereuse si elle n'est pas corrigée rapidement.
Utilisations de l'acétone:
Il existe de nombreuses utilisations pour l'acétone, mais celle que la plupart des gens connaissent est un ingrédient dans le dissolvant du vernis à ongles. L'acétone a de bonnes propriétés en tant que solvant et est donc également utile pour éliminer la peinture ou l'encre. Il est également parfois utilisé dans l'industrie pour faire certains types de fibres. Il a une certaine capacité à arrêter.
Sécurité à l'aide d'acétone:
Bien que généralement considéré comme sûr à utiliser dans la vie quotidienne, il a des propriétés potentiellement nocives. Par exemple, il est inflammable et les vapeurs peuvent provoquer une irritation des muqueuses comme les yeux. Vous devez éviter le contact avec la peau car il peut être irritant pour la peau.
Qu'est-ce que l'acétate?
Définition de l'acétate:
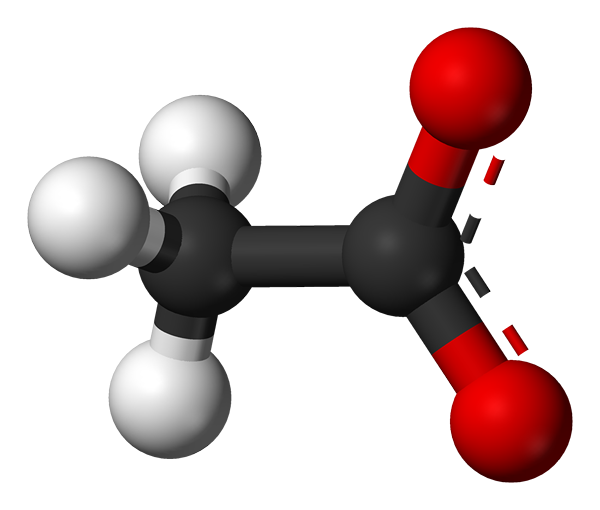
L'acétate est un anion qui est un acide monocarboxylique qui est formé à partir d'une modification chimique de l'acide acétique. La formule moléculaire de l'acétate est CH3COO ou (C2H3O2-). Le mot acétate est également un terme qui est souvent utilisé pour décrire un sel d'acétate.
Propriétés en acétate:
L'acétate a le poids moléculaire de 59.044 grammes par mol et il est classé comme un anion et parfois comme un sel lorsqu'il est combiné avec d'autres substances. En fait, certains sels acétates peuvent se dissoudre dans l'eau. De nombreuses propriétés de l'acétate seront influencées par les autres substances avec lesquelles ils réagissent ou se combinent, ce qui signifie qu'ils peuvent ou non être inflammables, par exemple.
Formation d'acétate:
La façon dont l'acétate peut être fabriquée est de combiner une substance particulière avec l'acide acétique. Plusieurs types d'acétates différents peuvent être formés en fonction de la substance combinée avec l'acide acétique. Il existe des organismes vivants tels que des bactéries méthanogènes du genre méthanosarcina qui sont capables de fabriquer de l'acétate lorsqu'elles sont cultivées sur certains substrats tels que la triméthylamine ou lorsqu'ils sont cultivés sur un substrat de méthanol.
Acétate utilise:
L'acétate est une substance utile lorsqu'elle est combinée avec d'autres substances. En fait, l'acétate d'éthyle peut être utilisé pour l'électroples et pour éliminer les vernis ou les peintures. L'acétate de cellulose peut être utilisé dans la fabrication de lunettes, et dans le passé, a également été utilisé dans le film photographique. Dans le monde naturel, l'acétate est utilisé pour fabriquer des acides gras.
Sécurité des acétate:
À quel point l'acétate est dangereux dépend de la substance avec laquelle il combine. Par exemple, l'acétate d'éthyle est une substance inflammable. D'un autre côté, lorsque la cellulose est combinée avec de l'acétate, un matériau non inflammable est produit.
Différence entre l'acétone vs acétate?
Définition
Une molécule d'acétone est une cétone qui a la formule CH3COCH3. L'acétate est un anion qui a la formule CH3COO-.
Masse moléculaire
L'acétone a un poids moléculaire de 58.07 grammes par mol. Le poids moléculaire de l'acétate est de 59.044 grammes par mole.
Type de molécule
L'acétone est classée comme un type de cétone, tandis que l'acétate est classé comme un type d'anion.
Nombre de groupes méthyle
Il y a deux groupes méthyles trouvés dans la molécule d'acétone. Il n'y a qu'un seul groupe méthyle trouvé dans la molécule d'acétate.
Nombre d'atomes d'oxygène
Il n'y a qu'un seul atome d'oxygène présent dans la molécule d'acétone. Il y a deux atomes d'oxygène trouvés dans la molécule d'acétate.
Formation dans l'industrie
L'acétone est fabriquée industriellement par une méthode appelée la méthode hydroperoxyde de Cumene. L'acétate est fabriqué lorsque l'acide acétique perd un proton et que les ions acétate sont souvent combinés avec d'autres substances pour former des sels.
Formation dans la nature
La formation d'acétone chez l'homme se produit par le catabolisme des graisses qui entraîne la production de cétones. La formation d'acétate se produit dans le monde vivant, avec certains organismes vivants, tels que les bactéries méthanogènes, capables de faire de l'acétate dans leurs cellules.
Odeur
L'acétone sent le plus de fruits, tandis que l'acétate peut sentir sucré ou comme de la colle.
Les usages
Il y a de nombreuses utilisations pour l'acétone, par exemple pour le déshabiller de la peinture ou des laques et enlever le vernis à ongles. Les utilisations de l'acétate incluent l'élimination du vernis ou de la peinture des surfaces et également pour la réalisation d'un film photographique. L'acétate est également souvent utilisé dans l'industrie de l'électroples.
Tableau comparant l'acétone vs. Acétate
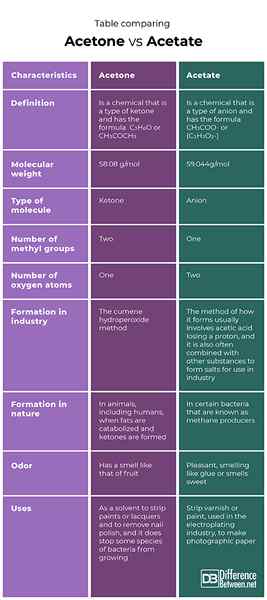
Résumé de l'acétone vs. Acétate
- L'acétone est une cétone couramment utilisée dans le dissolvant du vernis à ongles et même en tant que décapant de peinture.
- L'acétate est un anion qui peut également être utilisé pour éliminer la peinture des surfaces et est généralement combiné avec des molécules pour former d'autres substances utiles.
- L'acétone est une substance inflammable avec une odeur fruitée.
- L'acétate est parfois inflammable en fonction des substances avec lesquelles elle est combinée.

