Différence entre l'acétone et le benzaldéhyde
- 4756
- 688
- Théo Roy
Qu'est-ce que l'acétone?
L'acétone (diméthyl cétone, propanone) est un composé chimique, un liquide incolore, très inflammable et volatil, avec une odeur caractéristique. C'est la cétone la plus simple.
La formule chimique de l'acétone est C3H6O. Son poids moléculaire est de 58.08 g / mol.
Les vapeurs de l'acétone sont plus lourdes que l'air et leur densité liée à l'air est 2.0 (air = 1). L'acétone est moins dense que l'eau et sa densité liée à l'eau est 0.8 (eau = 1).
Dans les conditions de stockage recommandées, l'acétone est un composé stable. Son point d'ébullition est de 56 ° C et son point de fusion est de -95 ° C. L'auto-ingnition se produit à 465 ° C.

L'acétone se dissout bien dans l'eau. Il dissout un certain nombre de substances organiques polaires et non polaires ainsi que des substances inorganiques. Cette propriété détermine l'une des utilisations les plus importantes de l'acétone - comme solvant pour les vernis, plastiques, adhésifs, etc.
Les vapeurs d'acétone sont toxiques. Ils ont un effet narcotique et affectent le système nerveux central.
L'une des particularités importantes de l'acétone est sa capacité à s'accumuler dans le corps, augmentant ainsi sa concentration. Comme effet final d'une telle accumulation, un empoisonnement chronique peut se produire.
L'acétone se produit dans le corps humain, comme un produit de dégradation du métabolisme des graisses. Il se produit dans les plantes, les animaux, les échappements de véhicules, les gaz volcaniques, les incendies de forêt, etc.
Dans des circonstances normales, l'acétone se trouve en petites quantités dans l'urine et le sang. Après le jeûne ou le régime à long terme, la réserve de glucides dans le corps est épuisée, la graisse est décomposée, ce qui entraîne la production d'acétone et l'occurrence de la soi-disant «respiration d'acétone».
L'acétone se produit en plus grandes quantités dans le sang et l'urine des diabétiques. Des concentrations plus élevées d'acétone dans le corps entraînent une cétoacidose, qui est l'un des symptômes du diabète.
L'acétone est utilisée comme solvant dans une variété de réactions organiques, comme agent de séchage, et pour précipiter les protéines. Il est utilisé en médecine et cosmétique, pour les traitements d'acné pour peler la peau sèche. Il est largement utilisé pour dissolvant de vernis à ongles. L'acétone est également utilisée comme additif alimentaire - agent arôme. Il est utilisé dans la production de peintures et de revêtements. Il est souvent utilisé comme composant principal des agents de nettoyage.
Qu'est-ce que le benzaldéhyde?
Le benzaldéhyde est un liquide huileux, incolore à jaune avec une odeur d'amande. C'est un aldéhyde aromatique avec un seul groupe formyle. Il est contenu dans les pierres des amandes amères, des pêches, des cerises, etc. On peut parfois être trouvé dans l'urine humaine.
La formule chimique est de benzaldéhyde est c6H5Chou. Son poids moléculaire est de 106.124 g / mol.
Les vapeurs du benzaldéhyde sont plus lourdes que l'air, sa densité de vapeur liée à l'air est de 3.66 (air = 1). Il est légèrement plus dense que l'eau, sa densité liée à l'eau est 1.05 (eau = 1).
Le benzaldéhyde est un liquide réactif et devient jaunâtre sur. Son point d'ébullition est de 178.7 ° C et son point de fusion est de -57 ° C. L'auto-ingnition se produit à 192 ° C.
Le benzaldéhyde est insoluble dans l'eau et soluble dans l'ammoniac liquide.
Le benzaldéhyde peut être nocif s'il est avalé ou inhalé. Un contact prolongé avec la peau peut provoquer une irritation cutanée. Le contact avec les yeux provoque une grave irritation des yeux.
Le benzaldéhyde peut être obtenu à partir de diverses sources naturelles. Il est largement utilisé par l'industrie chimique dans la production d'arômes, de produits pharmaceutiques et de parfums. Il est également utilisé dans la préparation de différents colorants d'aniline, dans le traitement de l'eau et dans la production de carburants et d'additifs de carburant.
Différence entre l'acétone et le benzaldéhyde
Définition
Acétone: L'acétone est un composé chimique, un liquide incolore, très inflammable et volatil, avec une odeur caractéristique. C'est la cétone la plus simple.
Benzaldéhyde: Le benzaldéhyde est un liquide huileux, incolore à jaune avec une odeur d'amande. C'est un aldéhyde aromatique avec un seul groupe formyle.
Formule chimique
Acétone: La formule chimique de l'acétone est C3H6O.
Benzaldéhyde: La formule chimique est de benzaldéhyde est c6H5Chou.
Masse moléculaire
Acétone: Le poids moléculaire de l'acétone est de 58.08 g / mol.
Benzaldéhyde: Le poids moléculaire du benzaldéhyde est de 106.124 g / mol.
Vapeurs
Acétone: Les vapeurs de l'acétone sont plus lourdes que l'air et leur densité liée à l'air est 2.0 (air = 1).
Benzaldéhyde: Les vapeurs du benzaldéhyde sont plus lourdes que l'air, leur densité liée à l'air est 3.66 (air = 1).
Densité
Acétone: L'acétone est moins dense que l'eau et sa densité liée à l'eau est 0.8 (eau = 1).
Benzaldéhyde: Le benzaldéhyde est légèrement plus dense que l'eau, sa densité liée à l'eau est 1.05 (eau = 1).
La stabilité
Acétone: Dans les conditions de stockage recommandées, l'acétone est un composé stable.
Benzaldéhyde: Le benzaldéhyde est un liquide réactif et devient jaunâtre sur.
Point d'ébullition
Acétone: Le point d'ébullition de l'acétone est de 56 ° C.
Benzaldéhyde: Le point d'ébullition du benzaldéhyde est de 178.7 ° C.
Point de fusion
Acétone: Le point de fusion de l'acétone est de -95 ° C.
Benzaldéhyde: Le point de fusion du benzaldéhyde est de -57 ° C.
Auto-indication
Acétone: L'auto-indication de l'acétone se produit à 465 ° C.
Benzaldéhyde: L'auto-indication du benzaldéhyde se produit à 192 ° C.
Solubilité
Acétone: L'acétone se dissout bien dans l'eau.
Benzaldéhyde: Le benzaldéhyde est insoluble dans l'eau et soluble dans l'ammoniac liquide.
Dangers
Acétone: Les vapeurs d'acétone sont toxiques. Ils ont un effet narcotique et affectent le système nerveux central. L'une des particularités importantes de l'acétone est sa capacité à s'accumuler dans le corps, augmentant ainsi sa concentration. Comme effet final d'une telle accumulation, un empoisonnement chronique peut se produire.
Benzaldéhyde: Le benzaldéhyde peut être nocif s'il est avalé ou inhalé. Un contact prolongé avec la peau peut provoquer une irritation cutanée. Le contact avec les yeux provoque une grave irritation des yeux.
Occurrence
Acétone: L'acétone se produit dans le corps humain, comme un produit de dégradation du métabolisme des graisses. Il se produit dans les plantes, les animaux, les échappements de véhicules, les gaz volcaniques, les incendies de forêt, etc.
Benzaldéhyde: Le benzaldéhyde est contenu dans les pierres des amandes amères, des pêches, des cerises, etc. On peut parfois être trouvé dans l'urine humaine.
Utiliser
Acétone: L'acétone est utilisée comme solvant dans une variété de réactions organiques, comme agent de séchage, pour précipiter les protéines, comme agent aromatisant, dans la production de peintures, de revêtements, d'agents de nettoyage. Il est également utilisé en médecine et cosmétique.
Benzaldéhyde: Le benzaldéhyde est utilisé par l'industrie chimique dans la production d'arômes, de produits pharmaceutiques et de parfums. Il est également utilisé dans la préparation de différents colorants d'aniline, dans le traitement de l'eau et dans la production de carburants et d'additifs de carburant.
Versets d'acétone benzaldéhyde: tableau de comparaison
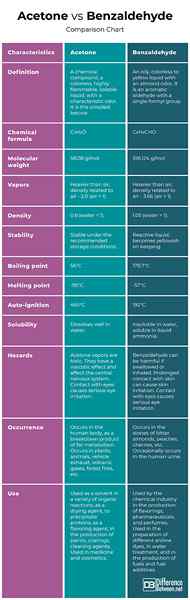
Résumé de l'acétone vs. Benzaldéhyde
- L'acétone est un composé chimique, un liquide incolore, très inflammable et volatil, avec une odeur caractéristique. C'est la cétone la plus simple.
- Le benzaldéhyde est un liquide huileux, incolore à jaune avec une odeur d'amande. C'est un aldéhyde aromatique avec un seul groupe formyle.
- La formule chimique de l'acétone est C3H6O, et la formule chimique est de benzaldéhyde est c6H5Chou.
- Le poids moléculaire de l'acétone est de 58.08 g / mol, tandis que le poids moléculaire du benzaldéhyde est 106.124 g / mol.
- Les vapeurs de l'acétone sont plus lourdes que l'air et leur densité liée à l'air est 2.0. Les vapeurs du benzaldéhyde sont également plus lourdes que l'air, et leur densité liée à l'air est 3.66 (air = 1).
- La densité de l'acétone liée à l'eau est 0.8, la densité du benzaldéhyde lié à l'eau est 1.05 (eau = 1).
- Dans les conditions de stockage recommandées, l'acétone est un composé stable. Le benzaldéhyde est un liquide réactif et devient jaunâtre sur.
- Le point d'ébullition de l'acétone est de 56 ° C. Le point d'ébullition du benzaldéhyde est de 178.7 ° C.
- Le point de fusion de l'acétone est de -95 ° C. Le point de fusion du benzaldéhyde est de -57 ° C.
- L'auto-indication de l'acétone se produit à 465 ° C, tandis que l'auto-indication du benzaldéhyde se produit à 192 ° C.
- L'acétone se dissout bien dans l'eau. Le benzaldéhyde est insoluble dans l'eau et est soluble dans l'ammoniac liquide.
- Les vapeurs d'acétone sont toxiques et affectent le système nerveux central. Le benzaldéhyde peut être nocif s'il est avalé ou inhalé. Un contact prolongé avec la peau peut provoquer une irritation cutanée.
- L'acétone se produit dans le corps humain, comme un produit de dégradation du métabolisme des graisses. Il se produit dans les plantes, les animaux, les échappements de véhicules, les gaz volcaniques, les incendies de forêt, etc. Le benzaldéhyde est contenu dans les pierres des amandes amères, des pêches, des cerises, etc. On peut parfois être trouvé dans l'urine humaine.
- L'acétone est utilisée comme solvant dans une variété de réactions organiques, comme agent de séchage, pour précipiter les protéines, comme agent aromatisant, dans la production de peintures, de revêtements, d'agents de nettoyage. Il est également utilisé en médecine et cosmétique. Le benzaldéhyde est utilisé par l'industrie chimique dans la production d'arômes, de produits pharmaceutiques et de parfums. Il est également utilisé dans la préparation de différents colorants d'aniline, dans le traitement de l'eau et dans la production de carburants et d'additifs de carburant.
- « Différence entre l'antivirus de Kaspersky et la sécurité Internet
- Différence entre l'antivirus McAfee et la sécurité Internet »

