Différence entre benzyl et phényle
- 3004
- 772
- Elisa Petit
Le groupe fonctionnel est un groupe d'atomes aux propriétés chimiques distinctes. Ces groupes sont responsables des propriétés chimiques caractéristiques des molécules qu'ils construisent.
Le benzyle et le phényle sont des groupes fonctionnels, contenant un cycle benzène.

Qu'est-ce que Benzyl?
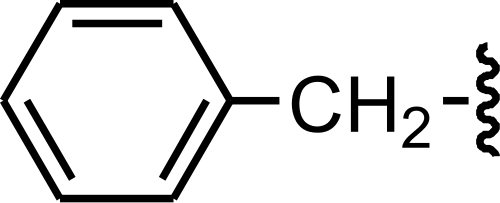
Le benzyl est un groupe fonctionnel, composé d'un anneau de benzène, attaché à un ch2 groupe. Sa formule chimique est C6H5Ch2-. Le benzyl est un radical monovalent dérivé du toluène.
L'abréviation «BN» est utilisée pour représenter le groupe benzyle. Par exemple, l'alcool benzylique peut être marqué comme bnoh.
La position du premier atome de C lié à une bague aromatique est décrite comme benzylique. Les positions benzyliques sont caractérisées par une réactivité améliorée. Il est dû à la faible énergie de dissociation des liaisons benzyl C - H. L'énergie, nécessaire pour la dissociation des liaisons de la liaison benzyl C-H, est de 90 kcal / mol, tandis que pour la liaison méthyl C-H, il est de 105 kcal / mol, et pour la liaison éthylique C-H, il est de 101 kcal / mol.
L'anneau aromatique a un rôle stabilisant pour les radicaux benzyliques. Cependant, la faible liaison C-H a un impact sur la stabilité du radical benzylique. En raison de la liaison C-H plus faible, les substituants benzyliques présentent une réactivité accrue de l'halogénation des radicaux libres, de l'oxydation, de l'hydrogénolyse, etc.
Les composés chimiques, contenant un groupe benzyle sont le benzyl méthyl, le bromure de benzyle, le chloroformate benzyle, la benzyl amine, etc.
Le benzyl est utilisé dans la synthèse organique comme groupe de protection pour les acides et les alcools carboxyliques.
Qu'est-ce que le phényle?
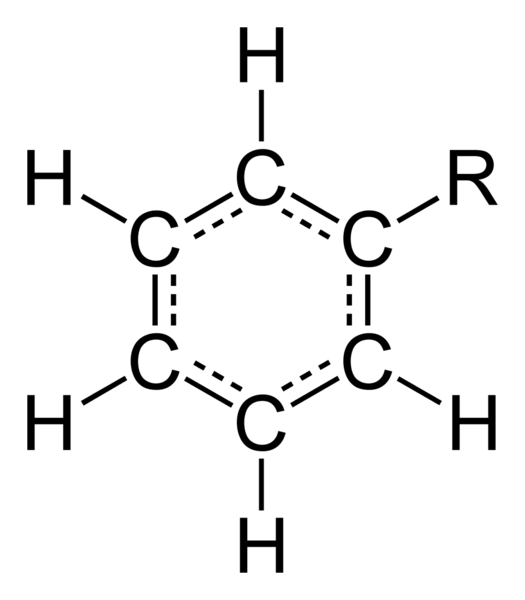
Le phényle est un groupe fonctionnel cyclique avec la formule C6H5-. Il s'agit d'un radical aryle monovalent, étroitement lié au benzène et en dérivé par élimination d'un atome H. Le groupe phényle a six atomes C liés dans un anneau hexagonal. L'un de ces atomes est lié à un substituant, et les cinq autres sont liés aux atomes d'hydrogène.
Le «pH» d'abréviation est utilisé pour représenter le groupe phényle. Par exemple, le benzène peut être désigné PHH.
L'énergie de dissociation des liaisons phényle C-H est supérieure à celle des autres liaisons C-H. L'énergie nécessaire à la dissociation des liaisons de la liaison phényle C-H est de 113 kcal / mol, tandis que pour la liaison méthyl C-H, il est de 105 kcal / mol, et pour la liaison éthyle C-H, il est de 101 kcal / mol.
Les propriétés des orbitales moléculaires aromatiques augmentent en outre la stabilité du groupe phényle. Les substances phényle sont hydrophobes et ont tendance à résister à la réduction et à l'oxydation.
Les composés chimiques, contenant le groupe phényle sont le triphénylméthane, le chlorobenzène, le phénol, etc.
Des composés contenant des groupes phényle sont utilisés dans le médicament. Par exemple, l'atorvastatine est utilisée pour réduire le cholestérol, la fexofénadine est utilisée pour traiter les allergies.
Différence entre benzyl et phényle
-
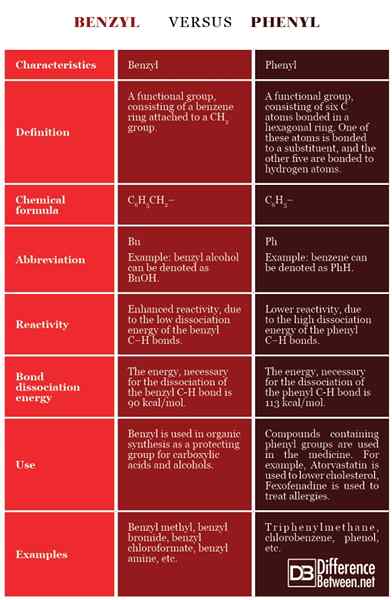
Définition
Benzyl: Le benzyl est un groupe fonctionnel, composé d'un anneau de benzène attaché à un ch2 groupe.
Phényle: Le phényle est un groupe fonctionnel composé de six atomes C liés dans un anneau hexagonal. L'un de ces atomes est lié à un substituant, et les cinq autres sont liés aux atomes d'hydrogène.
-
Formule chimique
Benzyl: La formule chimique du benzyl est C6H5Ch2-.
Phényle: La formule chimique du phényle est C6H5-.
-
Abréviation
Benzyl: L'abréviation «BN» est utilisée pour représenter le groupe benzyle. Par exemple, l'alcool benzylique peut être marqué comme bnoh.
Phényle: Le «pH» d'abréviation est utilisé pour représenter le groupe phényle. Par exemple, le benzène peut être désigné PHH.
-
Réactivité
Benzyl: Les positions benzyliques sont caractérisées par une réactivité accrue, en raison de la faible énergie de dissociation des liaisons benzyl C-H. Les substituants benzyliques présentent une réactivité accrue de l'halogénation des radicaux libres, de l'oxydation, de l'hydrogénolyse, etc.
Phényle: Les positions phényliques sont caractérisées par une réactivité plus faible, en raison de l'énergie de dissociation élevée des liaisons phényle C-H. Les substances phényle sont hydrophobes et ont tendance à résister à la réduction et à l'oxydation.
-
Énergie de dissociation des liaisons
Benzyl: L'énergie, nécessaire à la dissociation de la liaison benzyl C-H, est de 90 kcal / mol.
Phényle: L'énergie, nécessaire à la dissociation de la liaison phényle C-H, est de 113 kcal / mol.
-
Utiliser
Benzyl: Le benzyl est utilisé dans la synthèse organique comme groupe de protection pour les acides et les alcools carboxyliques.
Phényle: Des composés contenant des groupes phényle sont utilisés dans le médicament. Par exemple, l'atorvastatine est utilisée pour réduire le cholestérol, la fexofénadine est utilisée pour traiter les allergies.
-
Exemples
Benzyl: Les composés chimiques, contenant le groupe benzyle sont le benzyl méthyl, le bromure de benzyle, le chloroformate de benzyle, la benzyl amine, etc.
Phényle: Les composés chimiques, contenant le groupe phényle sont le triphénylméthane, le chlorobenzène, le phénol, etc.
Benzyl vs. Tableau de comparaison du phényle
Résumé de Benzyl VS. Phényle
- Le groupe fonctionnel est un groupe d'atomes aux propriétés chimiques distinctes.
- Le benzyl est un groupe fonctionnel, composé d'un anneau de benzène attaché à un ch2 groupe.
- Le phényle est un groupe fonctionnel composé de six atomes C liés dans un anneau hexagonal. L'un de ces atomes est lié à un substituant, et les cinq autres sont liés aux atomes d'hydrogène.
- La formule chimique du benzyl est C6H5Ch2-, tandis que la formule chimique du phényle est c6H5-.
- L'abréviation «BN» est utilisée pour représenter le groupe benzyle, tandis que l'abréviation «pH» est utilisée pour représenter le groupe phényle.
- Les positions benzyliques sont caractérisées par une réactivité accrue, en raison de la faible énergie de dissociation des liaisons benzyl C-H. Les positions phényliques sont caractérisées par une réactivité plus faible, en raison de l'énergie de dissociation élevée des liaisons phényle C-H.
- Les substituants benzyl présentent une réactivité accrue de l'halogénation des radicaux libres, de l'oxydation, de l'hydrogénolyse, etc. Les substances phényle sont hydrophobes et ont tendance à résister à la réduction et à l'oxydation.
- L'énergie, nécessaire à la dissociation de la liaison benzyl C-H, est de 90 kcal / mol. L'énergie, nécessaire à la dissociation de la liaison phényle C-H, est de 113 kcal / mol.
- Les composés chimiques, contenant le groupe benzyle sont le benzyl méthyl, le bromure de benzyle, le chloroformate de benzyle, la benzyl amine, etc. Les composés chimiques, contenant le groupe phényle sont le triphénylméthane, le chlorobenzène, le phénol, etc.
- « Différence entre le périphérique d'entrée et le périphérique de sortie
- Différence entre les isomères constitutionnels et les stéréoisomères »

