Différence entre cétone et ester
- 5005
- 864
- Lena Pons
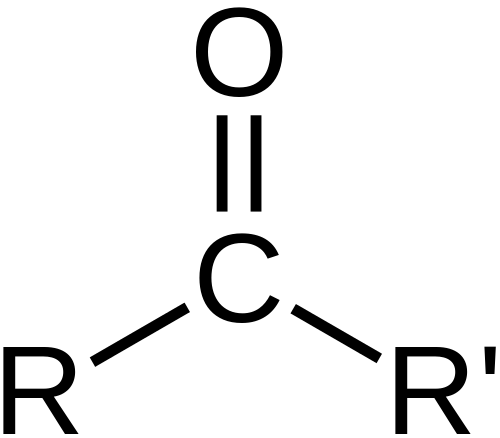
Un cétone a une structure moléculaire qui comprend un carbonyle lié aux carbones tandis qu'un ester a une structure moléculaire dans laquelle un carbonyle est lié à un groupe alcooxy.

Qu'est-ce que le cétone?
Définition:
Une cétone est une molécule dans laquelle un atome de carbone est lié de manière covalente à un atome d'oxygène pour faire un groupe carbonyle et les carbones sont liés à ce carbonyle.
Propriétés:
Les cétones sont des molécules qui ont une réactivité élevée et peuvent facilement réagir avec d'autres substances. Cela est dû à la nature très polaire du groupe carbonyle qui donne à son tour à la molécule une charge positive partielle. Cela signifie que d'autres substances sont souvent attirées par la molécule avec laquelle ils réagissent alors facilement. En fait, les réactions de l'addition nucléophile et de l'oxydation et de la réduction sont courantes.
Formation:
Il y a plusieurs façons dont un cétone peut être formé. De nombreux alcools et hydrocarbures peuvent être oxydés pour former des cétones. Les molécules appelées alcynes peuvent être modifiées par hydratation pour former des molécules de cétone.
Exemples et utilisations:
Il existe de nombreux exemples de cétones, notamment de l'acétone, de la phényléthanone et de la propanone. Les cétones constituent la base de la production de nombreux produits utiles dans l'industrie. Par exemple, ils sont souvent utilisés pour fabriquer divers solvants tels que l'acétone qui est largement utilisé comme dissolvant de vernis à ongles en raison de ses propriétés comme un excellent solvant. Les cétones peuvent également être utilisées pour dépouiller les peintures et les laques et même pour faire des explosifs et sont souvent utilisées dans l'industrie du bronzage.
Occurrence dans la nature:
Les corps cétone sont formés dans le corps humain lorsque les graisses sont métabolisées en cas de glucose insuffisant pour fournir l'énergie du corps. Chez les individus qui ont un diabète mal contrôlé lorsque des graisses excessives sont décomposées, ces cétones peuvent s'accumuler et la personne a donc souvent une respiration fruitée.
Qu'est-ce que l'ester?
Définition:
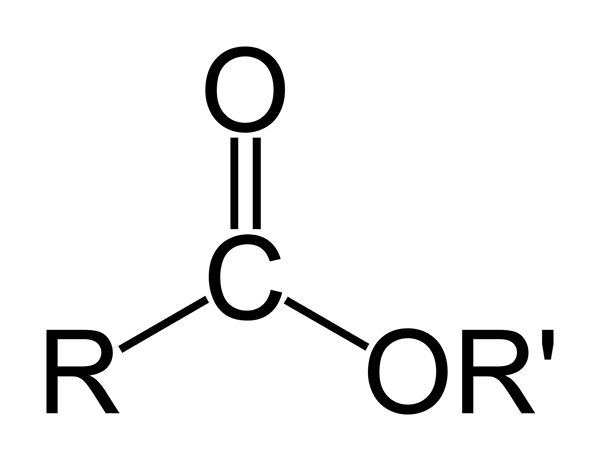
Un ester est une molécule qui a un groupe carbonyle et est une molécule dans laquelle l'hydroxyle a été remplacé par un groupe connu sous le nom d'alcoxy (un atome d'oxygène et un groupe alkyle).
Propriétés:
Les esters sont des molécules qui ont une polarité (en d'autres termes, ils ont une charge), et réagissent donc facilement avec d'autres molécules. De nombreux petits esters sont solubles dans l'eau mais l'étendue de la solubilité diminue à mesure que la taille de la molécule augmente. Les esters à longue chaîne sont donc insolubles dans l'eau et font partie de nombreuses molécules lipidiques. Un ester est moins acide qu'une cétone en raison de la présence du groupe alcooxy. Il est également moins réactif qu'une molécule de cétone.
Formation:
Les esters peuvent être formés à partir d'alcools, d'acides carboxyliques et certains des acides inorganiques tels que l'acide nitrique ou l'acide phosphorique. Le processus dans lequel l'acide carboxylique réagit avec l'eau en présence d'un certain type d'acide en présence de chaleur pour former un ester est appelé estérification.
Exemples et utilisations:
Il existe de nombreux exemples d'esters importants, comme par exemple, l'acétylcholine et l'acide ascorbique (vitamine C). L'acétate d'éthyle est un ester qui aide à donner de la saveur à la bière. Certains esters sont utilisés pour fabriquer une isolation par fil PVC car il rend l'isolation flexible. De nombreux esters d'acide tricarboxylique peuvent être trouvés dans le vin et aider à donner au vin une odeur spécifique. Les esters sont utilisés dans la fabrication de nombreuses substances, notamment en plexiglas et un film mylar. Différents esters sont utilisés pour fabriquer des colorants, des solvants et même des additifs à essence.
Occurrence dans la nature:
Les esters d'acides gras représentent bon nombre des différentes graisses qui se produisent dans la nature et se trouvent souvent chez les fruits. Les ananas et les bananes ont des esters qui donnent aux fruits une odeur spécifique. Les cires des plantes sont également un exemple d'ester qui se trouve dans la nature. Les esters de cholestérol pris par le régime alimentaire sont utilisés pour former du cholestérol chez les animaux, y compris chez l'homme.
Différence entre cétone et ester
Définition de cétone vs. Ester
Un cétone est une molécule qui a un carbonyle lié aux carbones. Un ester est une molécule qui a un groupe carbonyle et alcoxy lié ensemble.
Acidité
Une cétone est une molécule plus acide. Un ester est une molécule moins acide.
Réactivité
Les cétones ont plus de réactivité tandis que les esters ont moins de réactivité.
Formation
L'oxydation des alcools et des hydrocarbures peut produire une cétone comme peut l'hydratation des alcynes. La réaction d'estérification dans laquelle l'acide carboxylique et l'eau sont réagi peuvent produire un ester.
Usages industriels
Les cétones ont de nombreuses utilisations, notamment en tant que solvants tels que les déménageurs de vernis à ongles et les déménagements de peinture et de laque, et ils peuvent être utilisés pour produire des explosifs et dans l'industrie du bronzage. Les esters ont également plusieurs utilisations, notamment en tant que solvants, colorants, comme additifs dans l'essence et pour faire du film Mylar et du plexiglas.
Exemples chez l'homme
Les cétones sont formées lorsque les graisses sont décomposées s'il n'y a pas assez de glucose dans le corps pour produire de l'énergie. Les esters peuvent être pris par le régime alimentaire et utilisés pour former du cholestérol chez l'homme.
Tableau comparant le cétone et l'ester
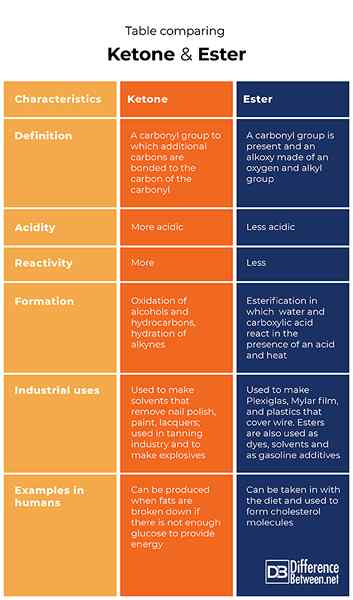
Résumé de la cétone vs. Ester
- Les cétones et les esters sont tous deux des molécules qui contiennent un groupe carbonyle, mais il existe différents atomes attachés au carbonyle dans chaque cas.
- Les cétones et les esters sont des molécules qui peuvent être utilisées comme solvants dans certaines situations.
- Les cétones sont plus réactives et acides que les esters.
- Les esters et les cétones se produisent tous deux dans les organismes vivants.

