Différence entre les propriétés physiques et chimiques
- 4029
- 498
- Hugo Marie

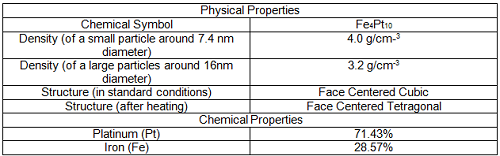
Qu'est-ce que les propriétés physiques?
Les propriétés physiques sont celles qui peuvent être observées et mesurées sans modifier la composition réelle de la question. La composition chimique et moléculaire reste la même quelle que soit la méthode de mesure utilisée.
Toute propriété qui peut être détectée et mesurée sans effectuer de réaction chimique est donc une propriété physique.
Des changements physiques peuvent se produire, e.g. changement d'états, mais cela ne change que la forme physique et non la structure chimique ou la composition moléculaire de la substance. Par exemple, lorsque l'eau gèle, la nature chimique de l'eau ne change pas, donc le point de congélation est une autre propriété physique.
Les états de matière sont également une propriété physique car toutes les substances peuvent exister dans une phase solide, liquide ou gazeuse en fonction de la perte d'énergie ou du gain.
Le même élément est présent après le changement et tout au long du processus. Les changements physiques sont liés aux propriétés physiques.
Les propriétés physiques peuvent être étendues ou intensives:
- Compenses étendues sur la quantité de matière mesurée, par exemple, la masse, le volume et la longueur.
Les propriétés étendues sont externes, c'est-à-dire que la substance ne peut pas être identifiée en utilisant celles-ci et les changements de valeur en fonction de la quantité de substance présente. Par exemple, vous pouvez mesurer 10 g d'huile ou 10 g d'eau, mais cela ne vous permet pas d'identifier une substance comme étant de l'huile ou de l'eau.
- Intensif - Ne dépendez pas de la quantité de matière mesurée, par exemple: couleur, densité, viscosité, flottabilité, point de fusion, point de congélation.
Les propriétés intensives sont toujours les mêmes et peuvent être utilisées pour identifier ce qu'est une substance. E.g. La densité de l'eau liquide est de 1 g / ml, le point d'ébullition est de 100oC et le point de congélation est 0oC.
L'utilisation de plusieurs propriétés intensives ensemble permet d'identifier une substance. Les substances peuvent également être classées et regroupées en fonction de leurs propriétés physiques.
Des exemples de propriétés physiques comprennent:
- Température
- Malléabilité
- Apparence
- Texture
- Couleur
- Odeur
- Forme
- Solubilité
- Charge électrique
- Masse moléculaire
- Point d'ébullition
- Point de fusion
- Point de congélation
- Volume
- Masse
- Longueur
- Densité
- Solubilité
- Polarité
- Viscosité
- Pression
- Charge électrique
- Dureté
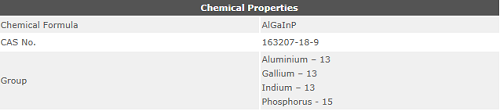
Qu'est-ce que les propriétés chimiques?
Une propriété chimique par définition signifie que la mesure de la propriété entraîne un changement dans la structure chimique réelle de la substance. Les propriétés chimiques deviennent apparentes lorsque la substance subit un changement ou une réaction chimique.
Les propriétés chimiques décrivent la capacité d'une substance à se combiner avec d'autres substances, ou se transformer en un produit différent. C'est une façon de décrire avec quoi une substance pourrait réagir ou finir par se transformer en. Lorsqu'une réaction chimique se produit, la matière se transforme en un type de matière entièrement différent.
Par exemple, le sodium peut réagir avec la vapeur d'eau dans l'air et exploser violemment; Le fer et l'oxygène se combinent pour former de la rouille, le fer a donc la capacité chimique à former de la rouille; L'essence a la capacité de brûler (elle est inflammable).
Une propriété chimique est toute qualité qui ne peut être établie que lorsqu'un changement est effectué dans l'identité chimique de la substance. Le simple fait de toucher ou d'observer une substance ne démontrera pas ses propriétés chimiques. La structure de la matière ou de la substance doit être modifiée afin de voir la propriété chimique.
Les propriétés chimiques sont utiles à savoir car cela aide à l'identification de substances inconnues ou lorsque vous essayez de séparer ou de purifier les substances, et peut permettre aux scientifiques de classer les substances telles que les composés.
Connaissant ces propriétés, les scientifiques peuvent proposer des applications où diverses substances peuvent être utilisées.
Les scientifiques sont également en mesure de prédire comment les échantillons réagiront dans une réaction chimique s'ils ont une connaissance préalable des propriétés chimiques des substances.
Quelques exemples de propriétés chimiques comprennent les éléments suivants:
- Toxicité
- Stabilité chimique (si un composé réagira avec de l'eau ou de l'air)
- Chaleur de combustion
- Inflammabilité (si le composé brûlera lorsqu'il sera exposé à la flamme)
- Réactivité (capacité à réagir avec d'autres produits chimiques)
- Enthalpie de formation
- États d'oxydation (gagner de l'oxygène, perdre de l'hydrogène ou perdre des électrons, et entraînant le nombre d'oxydation d'une substance modifiée. Un exemple de cela serait de la rouille).
- Types de liaisons chimiques qui se formeront (qu'elles soient covalentes, non covalentes ou hydrogène)
- Flottabilité
- Viscosité
- Compressibilité
- Radioactivité (émission de rayonnement à partir d'un atome)
- Demi-vie
Quelle est la différence entre les propriétés physiques et chimiques?
- Les propriétés physiques sont les propriétés qui peuvent être observées ou mesurées sans
provoquant ou entraînant un changement dans la question, alors que les propriétés chimiques ne sont observées qu'après qu'un changement de la matière s'est produit.
- Les propriétés physiques peuvent changer les états sans changer la structure moléculaire, mais ce n'est pas le cas des propriétés chimiques.
- Avec les propriétés chimiques que l'identité chimique de la substance est modifiée, ce n'est pas le cas avec les propriétés physiques.
- Avec les propriétés chimiques, la structure du matériau change, tandis que la structure ne change pas dans le cas des propriétés physiques.
- Une réaction chimique se produit avant qu'une propriété chimique ne devienne évidente, alors qu'aucune réaction chimique n'est nécessaire pour qu'une propriété physique devienne visible.
- Les propriétés chimiques, contrairement aux propriétés physiques, peuvent être utilisées pour prédire comment les substances réagiront.
Tableau comparant les propriétés physiques et chimiques
| Propriété physique | Propriété chimique |
| Observé sans apporter un changement | Seulement observé après avoir apporté un changement |
| Peut changer l'état physique mais pas les molécules | Change toujours les molécules |
| L'identité chimique reste la même | Changements d'identité chimique |
| La structure du matériau ne change pas | Structure des changements de matériaux |
| Aucune réaction chimique n'est nécessaire pour montrer la propriété | Une réaction chimique est nécessaire pour montrer la propriété |
| Ne peut pas être utilisé pour prédire comment les substances réagiront | Peut être utilisé pour prédire comment les substances réagiront |
Résumé:
- Des propriétés physiques peuvent être observées sans avoir à subir de changement en la matière.
- Les propriétés physiques peuvent varier en fonction de la quantité de matière, par exemple, la longueur, le volume et la masse. Ceux-ci sont connus sous le nom de propriétés physiques étendues.
- Les propriétés physiques intensives ne dépendent pas de la quantité de matière, e.g. texture.
- Les propriétés physiques peuvent changer les états tout en conservant la même structure chimique, E.g. congélation ou bouillir à l'eau.
- Les propriétés chimiques ne peuvent être observées qu'avec un changement, comme une réaction chimique.
- La matière est classée à la fois en fonction de leurs propriétés physiques et chimiques.
- « Différence entre l'eau mousseuse et l'eau de soude
- Différence entre un interrupteur géré et non géré »

